GLP-1
GLP-1: Die Brücke zwischen Glukose, Sättigung und Körpergewicht
In der aktuellen Landschaft der metabolischen Gesundheit nimmt GLP-1 eine zentrale Stellung ein. Seine wachsende Bedeutung innerhalb der wissenschaftlichen Gemeinschaft zeigt sich unter anderem in der Entwicklung von Arzneimitteln, die auf seinen Rezeptor abzielen. Über seine therapeutische Anwendung hinaus stellt sich jedoch eine grundlegendere Frage: Welche Rolle spielt GLP-1 als Regulator des Stoffwechsels?
Weit davon entfernt, lediglich ein „Gewichtsreduktionshormon“ zu sein, übernimmt das Glucagon-like Peptide-1 (GLP-1) eine zentrale Rolle in der koordinierten Regulation von Glukosestoffwechsel, Appetitkontrolle und Energiebilanz (1,2). Das Verständnis dieser Achse ermöglicht eine systemischere Betrachtung des Stoffwechsels.
Ein Hormon mit
abgestimmter Funktion
GLP-1 ist ein Inkretin-Hormon, , das von speziellen Zellen in der Darmschleimhaut gebildet wird, die sich hauptsächlich im Ileum und Kolon befinden. Nach seiner Ausschüttung zirkuliert es in zwei aktiven Hauptformen – GLP-1 (7–36) und GLP-1 (7–37) – und weist aufgrund des schnellen Abbaus durch das Enzym DPP-IV eine kurze Halbwertszeit auf (1).
Seine biologische Wirkung entsteht durch die Bindung an den GLP-1-Rezeptor (GLP-1R), der in verschiedenen Geweben vorkommt. Die Aktivierung dieses Rezeptors löst eine intrazelluläre, cAMP-abhängige Signalübertragung aus, die (1,3):
die glukoseabhängige Insulinsekretion stimuliert,
die Glukagonfreisetzung hemmt,
die funktionelle Masse der pankreatischen β-Zellen erhält,
die Blutzuckerregulierung verbessert.
Dieser Mechanismus positioniert GLP-1 als zentralen Modulator der metabolischen Kontrolle.
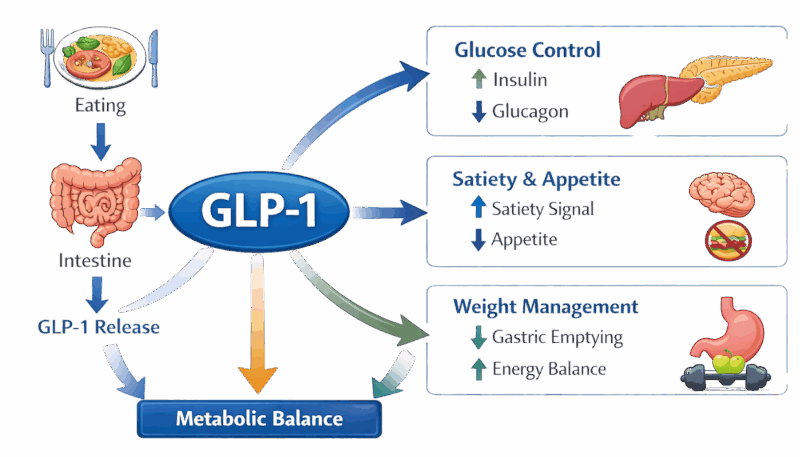
Konzeptuelles Schema basierend auf (Wang et al., 2021; Domínguez-Avila et al., 2017; Derosa et al., 2025).
Ausgangspunkt: Glukoseregulation
Angesichts der breiten medialen Aufmerksamkeit für GLP-1-Analoga wie Semaglutid (Ozempic) und Liraglutid (Saxenda) konzentriert sich die öffentliche Diskussion weitgehend auf deren Wirkung zur Gewichtsreduktion. Diese Betonung hat jedoch die primäre physiologische Rolle von GLP-1 etwas in den Hintergrund gedrängt: die Regulation der postprandialen Glukose, also die Kontrolle des Anstiegs des Blutzuckerspiegels nach der Nahrungsaufnahme.
Eine gleichmäßigere Entwicklung des Blutzuckerspiegels nach einer Mahlzeit reduziert Schwankungen in Stoffwechselprozessen und verhindert eine überhöhte Insulinfreisetzung als Gegenreaktion – zwei Faktoren, die eng mit der fortschreitenden Entwicklung von Insulinresistenz und Typ-2-Diabetes verbunden sind. In diesem Zusammenhang ist nicht allein die Höhe des Glukoseanstiegs entscheidend, sondern die Effizienz, mit der der Körper diesen Anstieg reguliert und sich daran anpasst (2,4,5).
Typ-2-Diabetes entsteht nicht abrupt, sondern entwickelt sich allmählich, wenn periphere Gewebe weniger empfindlich auf Insulin reagieren und die pankreatischen β-Zellen einen fortschreitenden funktionellen Rückgang erfahren. Treffen diese Prozesse zusammen, wird die Aufrechterhaltung der glykämischen Homöostase beeinträchtigt.
Vor diesem Hintergrund gewinnt das Inkretinsystem, insbesondere die GLP-1/GLP-1R-Achse, erhebliche physiologische Bedeutung (1,3,6). GLP-1 verstärkt die glukoseabhängige Insulinsekretion, das heißt, seine Wirkung nimmt zu, wenn die Glukosekonzentration nach einer Mahlzeit steigt, während gleichzeitig die Glukagonfreisetzung unterdrückt wird. Diese koordinierte Reaktion ermöglicht eine physiologisch angemessenere metabolische Anpassung, trägt zum Erhalt der β-Zell-Funktion bei und verbessert die gesamte metabolische Regulation (1,6).
Dementsprechend gehen Strategien zur Optimierung der postprandialen Blutzuckerkontrolle über eine bloße Gewichtsreduktion hinaus.
Sie zielen darauf ab, die Qualität und Effizienz der metabolischen Reaktion auf jede Mahlzeit zu verbessern – ein Ansatz mit weitreichenden Implikationen für die Prävention und das langfristige Management metabolischer Störungen (2,7,8).
GLP-1 und Sättigung: Die Darm–Gehirn-Verbindung
Über seine Rolle bei der Blutzuckerkontrolle hinaus ist GLP-1 direkt an der Appetitregulation beteiligt. Das Hormon verlangsamt die Magenentleerung, verlängert das Sättigungsgefühl nach Mahlzeiten und wirkt auf Nervenzellen im Gehirn, die den GLP-1-Rezeptor tragen. Dadurch werden Sättigungssignale beeinflusst und die Nahrungsaufnahme reduziert (1).
Dieser Effekt ist Teil eines Rückkopplungssystems, das die Energiebilanz entsprechend dem Ernährungszustand anpasst. Während des Fastens steigen die Ghrelinspiegel und regen den Appetit an; nach der Nahrungsaufnahme steigt die GLP-1-Sekretion und hilft, dieses appetitanregende Signal zu dämpfen. Die wechselseitige Interaktion dieser Hormone zeigt eine koordinierte Regulation der Energiebilanz und verdeutlicht, dass GLP-1 nicht nur auf Glukose, sondern auf den gesamten metabolischen Zustand des Organismus reagiert (1).
Mikrobiota und GLP-1
Die Fermentation von Ballaststoffen durch die Darmmikrobiota erzeugt kurzkettige Fettsäuren (SCFAs), die die GLP-1-Sekretion modulieren können (6). Diese Beziehung unterstreicht die Rolle des Darms als zentrales Organ im Hormonsystem bei der Regulation des Stoffwechsels und zeigt, dass die Wechselwirkung zwischen Ernährung, Mikrobiota und Inkretinen wichtig für die Vorbeugung von Herz-Kreislauf- und Stoffwechselerkrankungen ist (8,9).
Regulation der GLP-1-Sekretion: Ein multifaktorielles System
Die GLP-1-Sekretion reagiert auf ein integriertes System aus neuronalen und nutritiven Signalen.
Nach der Nahrungsaufnahme erfolgt zunächst eine frühe Phase, die durch Signale vom Nervensystem zwischen Darm und Gehirn sowie durch Hormone vermittelt wird, gefolgt von einer zweiten Phase, die vom direkten Kontakt der Nährstoffe mit dem Darm abhängt (1). In dieser zweiten Phase stimulieren Glukose, Fettsäuren, von der Mikrobiota produzierte SCFAs sowie Peptide oder Aminosäuren die intestinalen L-Zellen über spezifische Rezeptoren und Transporter (1,7).
Dieses Modell bestätigt, dass GLP-1 als metabolischer Sensor der Nährstoffaufnahme fungiert.
Angepasst nach (Wang et al., 2021; Domínguez-Avila et al., 2017; Iatcu et al., 2024).
Obwohl seine primäre Rolle in der Blutzuckerkontrolle liegt, entfaltet GLP-1 auch Wirkungen in anderen Geweben mit potenzieller Bedeutung für die Leberfunktion, die kardiovaskuläre Regulation und den Knochenstoffwechsel (1). Insgesamt kann die GLP-1/GLP-1R-Achse als integrativer Knotenpunkt verstanden werden, der Darm, Pankreas und zentrales Nervensystem in der Regulation des metabolischen Gleichgewichts miteinander verbindet.
Suchen Sie nach den passenden Inhaltsstoffen?
Abonnieren Sie unseren Newsletter…
…oder entdecken Sie unsere Inhaltsstoffe in folgendem Produktportfolio!
Quellen
- Wang Y, Alkhalidy H, Liu D. The emerging role of polyphenols in the management of type 2 diabetes. Molecules. 2021;26(3):703.
- Derosa G, et al. Nutraceuticals and supplements in the management of prediabetes and diabetes: Mechanistic and clinical evidence. Nutrients. 2025;17(1):14.
- Domínguez Avila JA, et al. The antidiabetic mechanisms of polyphenols related to increased GLP-1 and insulin signaling. Molecules. 2017;22(6):903.
- Lown M, Fuller R, Lightowler H, Fraser A, Gallagher A. Mulberry-extract improves glucose tolerance and decreases insulin concentrations in normoglycaemic adults: A randomized double-blind placebo-controlled study. PLoS ONE. 2017;12(2):e0172239.
- Thondre PS, Lightowler H, Ahlstrom L. Mulberry leaf extract improves glycaemic response to sucrose in healthy subjects: A randomized, double-blind, placebo-controlled study. Nutrition & Metabolism. 2021;18:42.
- Abiola JO, et al. Potential role of phytochemicals as GLP-1 receptor agonists in diabetes. Pharmaceuticals. 2024;17(6):736.
- Iatcu OC, et al. Harnessing prebiotics to improve type 2 diabetes outcomes: Mechanisms and clinical relevance. Nutrients. 2024;16(20):3447.
- Venkatakrishnan K, et al. Functional foods and nutraceuticals in obesity and metabolic disorders. Food & Function. 2019;10:1240–1263.
- Cevallos-Fernández E, et al. Fermented plant-based foods and postbiotics for glycemic control: Mechanistic insights and clinical implications. Frontiers in Nutrition. 2026.






